Giải Hóa 10 Bài 16: Các yếu tố ảnh hưởng đến tốc độ phản ứng hóa học
Câu hỏi 1 trang 98 Hóa học 10: Tiến hành thí nghiệm 1 và quan sát hiện tượng của thí nghiệm. Nhận xét mối liên hệ giữa thể tích dung dịch Na2S2O3 với thời gian xuất hiện kết tủa.
Thí nghiệm 1: Ảnh hưởng của nồng độ đến tốc độ phản ứng
Hóa chất: Dung dịch sodium thiosulfate (Na2S2O3) 0,15M; sulfuric acid (H2SO4) 0,10M; nước cất.
Dụng cụ: cốc thủy tinh 100 mL (được đánh dấu thập ở mặt ngoài đáy cốc), ống đong 50 mL.
Tiến hành:
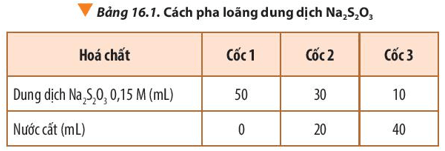
Bước 1: Pha loãng dung dịch Na2S2O3 0,15 M để được các dung dịch có nồng độ khác nhau theo Bảng 16.1.
Bước 2: Rót đồng thời 10 mL dung dịch H2SO4 0,1 M vào mỗi cốc và khuấy đều.
Phương trình hóa học của phản ứng:
Na2S2O3(aq) + H2SO4(aq) → Na2SO4(aq) + S(s) + SO2(g) + H2O(l)
Lời giải:
Thể tích dung dịch Na2S2O3 0,15 M càng nhỏ ⇒ Nồng độ Na2S2O3 càng nhỏ (hay dung dịch Na2S2O3 càng loãng) ⇒ Thời gian xuất hiện kết tủa càng lâu.
Xem thêm lời giải bài tập Hóa học lớp 10 Chân trời sáng tạo hay, chi tiết khác: