Hóa 10 Kết nối tri thức Bài 2: Nguyên tố hóa học
Giải Hóa học 10 | No tags
Mục lục
- Đang tải mục lục...
Các nguyên tử có cùng số đơn vị điện tích hạt nhân thì có đặc điểm gì chung?
Giải Hóa 10 Bài 2: Nguyên tố hóa học
Mở đầu trang 17 Hóa học 10: Các nguyên tử có cùng số đơn vị điện tích hạt nhân thì có đặc điểm gì chung? Giữa số đơn vị điện tích hạt nhân, số proton và số electron có mối liên hệ như thế nào?
Lời giải:
- Các nguyên tử có cùng số đơn vị điện tích hạt nhân thì thuộc cùng một nguyên tố hóa học và có tính chất hóa học tương tự nhau.
- Số đơn vị điện tích hạt nhân = số proton = số electron.
Xem thêm lời giải bài tập Hóa học lớp 10 Kết nối tri thức hay, chi tiết khác:
Cho các nguyên tử sau: L (Z = 8, A = 16), D (Z = 9, A = 19)
Giải Hóa 10 Bài 2: Nguyên tố hóa học
Câu hỏi 1 trang 17 Hóa học 10: Cho các nguyên tử sau: L (Z = 8, A = 16), D (Z = 9, A = 19), E (Z = 8, A = 18), G (Z = 7, A = 15). Trong các nguyên tử trên, các nguyên tử nào thuộc cùng một nguyên tố hóa học?
Lời giải:
Các nguyên tử thuộc cùng một nguyên tử hóa học khi có cùng số đơn vị điện tích hạt nhân Z ⇒ Các nguyên tử L và E thuộc cùng một nguyên tố hóa học (đều có Z = 8).
Xem thêm lời giải bài tập Hóa học lớp 10 Kết nối tri thức hay, chi tiết khác:
Kí hiệu một nguyên tử cho biết những thông tin gì? Cho ví dụ
Giải Hóa 10 Bài 2: Nguyên tố hóa học
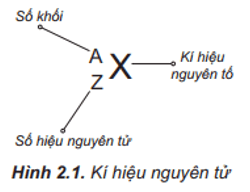
Câu hỏi 2 trang 18 Hóa học 10: Kí hiệu một nguyên tử cho biết những thông tin gì? Cho ví dụ.
Lời giải:
- Kí hiệu nguyên tử cho biết kí hiệu nguyên tố, số khối và số hiệu nguyên tử.
Thông qua kí hiệu nguyên tử xác định được thành phần các hạt có trong nguyên tử.
- Ví dụ: Kí hiệu nguyên tử cho biết:
+ Kí hiệu nguyên tố là Fe.
+ Số khối bằng 56.
+ Số hiệu nguyên tử (số đơn vị điện tích hạt nhân nguyên tử) là 26 nên trong hạt nhân nguyên tử sắt có 26 proton, vỏ nguyên tử sắt có 26 electron; số khối của nguyên tử Fe là 56 nên trong hạt nhân số neutron là 56 – 26 = 30.
Xem thêm lời giải bài tập Hóa học lớp 10 Kết nối tri thức hay, chi tiết khác:
Hãy biểu diễn kí hiệu của một số nguyên tử sau
Giải Hóa 10 Bài 2: Nguyên tố hóa học
Câu hỏi 3 trang 18 Hóa học 10: Hãy biểu diễn kí hiệu của một số nguyên tử sau:
a) Nitrogen (số proton = 7 và số neutron = 7).
b) Phosphorus (số proton = 15 và số neutron = 16).
c) Copper (đồng) (số proton = 29 và số neutron = 34).
Lời giải:
a) Nitrogen
Số hiệu nguyên tử = số proton = 7
Số khối = số proton + số neutron = 7 + 7 = 14
⇒ Kí hiệu nguyên tử:
b) Phosphorus
Số hiệu nguyên tử = số proton = 15
Số khối = số proton + số neutron = 15 + 16 = 31
⇒ Kí hiệu nguyên tử:
c) Copper
Số hiệu nguyên tử = số proton = 29
Số khối = số proton + số neutron = 29 + 34 = 63
⇒ Kí hiệu nguyên tử:
Xem thêm lời giải bài tập Hóa học lớp 10 Kết nối tri thức hay, chi tiết khác:
Xác định thành phần nguyên tử (số proton, neutron, electron) của mỗi đồng vị sau
Giải Hóa 10 Bài 2: Nguyên tố hóa học
Câu hỏi 4 trang 18 Hóa học 10: Xác định thành phần nguyên tử (số proton, neutron, electron) của mỗi đồng vị sau:
a)
b)
Lời giải:
Áp dụng:
Trong nguyên tử:
+ Số hiệu nguyên tử Z = số proton = số electron.
+ Số neutron = Số khối A – số hiệu nguyên tử Z.
a)
|
|||
Số proton |
14 | 14 | 14 |
Số electron |
14 | 14 | 14 |
Số neutron |
14 | 15 | 16 |
b)
|
||||
Số proton |
26 | 26 | 26 | 26 |
Số electron |
26 | 26 | 26 | 26 |
Số neutron |
28 | 30 | 31 | 32 |
Xem thêm lời giải bài tập Hóa học lớp 10 Kết nối tri thức hay, chi tiết khác:
Tỉ lệ phần trăm số nguyên tử các đồng vị của neon (Ne) được xác định theo phổ
Giải Hóa 10 Bài 2: Nguyên tố hóa học
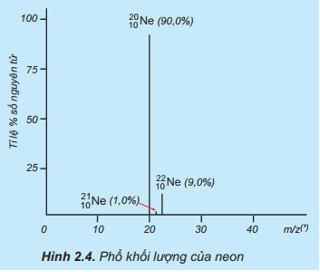
Câu hỏi 5 trang 20 Hóa học 10: Tỉ lệ phần trăm số nguyên tử các đồng vị của neon (Ne) được xác định theo phổ khối lượng (Hình 2.4). Tính nguyên tử khối trung bình của Ne.
Lời giải:
Nguyên tử khối trung bình của Ne là:
Xem thêm lời giải bài tập Hóa học lớp 10 Kết nối tri thức hay, chi tiết khác:
Vì sao trong bảng tuần hoàn các nguyên tố hóa học, giá trị nguyên tử khối của chromium
Giải Hóa 10 Bài 2: Nguyên tố hóa học
Câu hỏi 6 trang 20 Hóa học 10: Vì sao trong bảng tuần hoàn các nguyên tố hóa học, giá trị nguyên tử khối của chromium (Cr) không phải là số nguyên, mà là 51,996?
Lời giải:
Chromium có 4 nguyên tử đồng vị trong tự nhiên đó là 50Cr; 52Cr; 53Cr và 54Cr.
⇒ Nguyên tử khối trung bình của chromium không phải là số nguyên mà là 51,996.
Xem thêm lời giải bài tập Hóa học lớp 10 Kết nối tri thức hay, chi tiết khác:
Copper (đồng) được sử dụng làm dây dẫn điện, huy chương, trống đồng
Giải Hóa 10 Bài 2: Nguyên tố hóa học
Câu hỏi 7 trang 20 Hóa học 10: Copper (đồng) được sử dụng làm dây dẫn điện, huy chương, trống đồng, … Nguyên tử khối trung bình của copper bằng 63,546. Copper tồn tại trong tự nhiên dưới hai dạng đồng vị và . Tính phần trăm số nguyên tử của đồng vị tồn tại trong tự nhiên.
Lời giải:
Gọi phần trăm số nguyên tử của đồng vị tồn tại trong tự nhiên là x %.
⇒ Phần trăm số nguyên tử của là 100 – x (%)
Ta có:
Xem thêm lời giải bài tập Hóa học lớp 10 Kết nối tri thức hay, chi tiết khác:
Xác định được: nguyên tử khối, nguyên tử khối trung bình và phần trăm số nguyên tử
Giải Hóa 10 Bài 2: Nguyên tố hóa học
Em có thể 1 trang 20 Hóa học 10: Xác định được: nguyên tử khối, nguyên tử khối trung bình và phần trăm số nguyên tử các đồng vị của một nguyên tố hóa học.
Lời giải:
Ví dụ: Trong tự nhiên, chlorine có hai đồng vị bền là (chiếm 75,77%) và (chiếm 24,23%).
Ta xác định được:
- Đồng vị và có nguyên tử khối lần lượt là 35 và 37.
- Nguyên tử trung bình của nguyên tố chlorine là
Xem thêm lời giải bài tập Hóa học lớp 10 Kết nối tri thức hay, chi tiết khác:
Giải thích được vì sao nguyên tử khối của các nguyên tố hóa học
Giải Hóa 10 Bài 2: Nguyên tố hóa học
Em có thể 2 trang 20 Hóa học 10: Giải thích được vì sao nguyên tử khối của các nguyên tố hóa học không phải là các trị số nguyên và hiểu được sự đa dạng của nguyên tố hóa học trong tự nhiên thông qua khái niệm đồng vị.
Lời giải:
- Nguyên tử khối của các nguyên tố hóa học không phải là các trị số nguyên vì các nguyên tố đều có ít nhất từ 2 đồng vị khác nhau và có số phần trăm số nguyên tử xác định.
- Đồng vị là những nguyên tử có cùng số đơn vị điện tích hạt nhân (cùng số proton) nhưng khác nhau số neutron. Nguyên tố hóa học là tập hợp các nguyên tử có cùng số đơn vị điện tích hạt nhân ⇒ Trong tự nhiên đã phát hiện được 94 nguyên tố.
Xem thêm lời giải bài tập Hóa học lớp 10 Kết nối tri thức hay, chi tiết khác: